高校化学/有機/有機化合物の基礎・異性体

問題文をクリックすると解答が表示されます。
炭素
低い
(1) 鎖式 (2) 環式
(1) 鎖式(脂肪族) (2) 環式 (3) 芳香族 (4) 脂環式 (5) 飽和 (6) 不飽和
(1) メチル (2) アルキル
(1) 官能 (2) 示性
(1) 塩化カルシウムCaCl2 (2) 水 (3) ソーダ石灰 (4)二酸化炭素
(1) 一酸化炭素 (2) 酸化鉄(Ⅱ) (3) 酸化 (4) 二酸化炭素
(1) 組成式(実験式) (2) 分子量 (3) 分子式
(1) 中 (2) アルキル (3) フェニル
(1) 酸 (2) 塩基 (3) 中
(1) 窒素 (2) 硫黄 (3) 塩素
(ア) 弱酸性で,アルコールと反応して芳香性物質をつくる。
(イ) 強酸性で,塩基と反応して塩をつくる。
(ウ) 弱塩基性で,酸と反応して塩をつくる。
(エ) 水によく溶け,中性である。ナトリウムと反応する。
(オ) 中性で,還元するとアミノ基になる。
(カ) フェーリング溶液を還元して, 赤色沈殿をつくる。
(キ) 臭素水を脱色する。
(ク) 水素で還元すると,第二級アルコールになる。
(ア)
(ア) 弱酸性で,アルコールと反応して芳香性物質をつくる。
(イ) 強酸性で,塩基と反応して塩をつくる。
(ウ) 弱塩基性で,酸と反応して塩をつくる。
(エ) 水によく溶け,中性である。ナトリウムと反応する。
(オ) 中性で,還元するとアミノ基になる。
(カ) フェーリング溶液を還元して, 赤色沈殿をつくる。
(キ) 臭素水を脱色する。
(ク) 水素で還元すると,第二級アルコールになる。
(ウ)
(ア) 弱酸性で,アルコールと反応して芳香性物質をつくる。
(イ) 強酸性で,塩基と反応して塩をつくる。
(ウ) 弱塩基性で,酸と反応して塩をつくる。
(エ) 水によく溶け,中性である。ナトリウムと反応する。
(オ) 中性で,還元するとアミノ基になる。
(カ) フェーリング溶液を還元して, 赤色沈殿をつくる。
(キ) 臭素水を脱色する。
(ク) 水素で還元すると,第二級アルコールになる。
(ク)
(ア) 弱酸性で,アルコールと反応して芳香性物質をつくる。
(イ) 強酸性で,塩基と反応して塩をつくる。
(ウ) 弱塩基性で,酸と反応して塩をつくる。
(エ) 水によく溶け,中性である。ナトリウムと反応する。
(オ) 中性で,還元するとアミノ基になる。
(カ) フェーリング溶液を還元して, 赤色沈殿をつくる。
(キ) 臭素水を脱色する。
(ク) 水素で還元すると,第二級アルコールになる。
(イ)
(ア) 弱酸性で,アルコールと反応して芳香性物質をつくる。
(イ) 強酸性で,塩基と反応して塩をつくる。
(ウ) 弱塩基性で,酸と反応して塩をつくる。
(エ) 水によく溶け,中性である。ナトリウムと反応する。
(オ) 中性で,還元するとアミノ基になる。
(カ) フェーリング溶液を還元して, 赤色沈殿をつくる。
(キ) 臭素水を脱色する。
(ク) 水素で還元すると,第二級アルコールになる。
(オ)
(ア) 弱酸性で,アルコールと反応して芳香性物質をつくる。
(イ) 強酸性で,塩基と反応して塩をつくる。
(ウ) 弱塩基性で,酸と反応して塩をつくる。
(エ) 水によく溶け,中性である。ナトリウムと反応する。
(オ) 中性で,還元するとアミノ基になる。
(カ) フェーリング溶液を還元して, 赤色沈殿をつくる。
(キ) 臭素水を脱色する。
(ク) 水素で還元すると,第二級アルコールになる。
(カ)
化合物を構成する元素の種類や、その物質比を決めることを( 1 )という。
炭素,水素,酸素のみから なる有機化合物の (1) は, 次のように行うことができる。
すなわち,質量を正確に測定した試料を完全燃焼させ, 生成した H2O を( 2 )を詰めた管(H2O 吸収管)に, CO2を( 3 )を詰めた管(CO2 吸収管) に吸収させる。
Hk2O 吸収管および CO2 吸収管の質量増加から, 生成した H2O および CO2 の質量を求め, 試料中の CとHの質量を計算する。
そして,試料中の O の質量を計算したのち,その化合物に含まれる原子の数の比を最も簡単な整数の比で表した( 4 )が決定される。
さらに,( 5 )などを利用して( 6 )を求め,(4)を整数倍することにより分子式 が求められる。
(1) 元素分析 (2) 塩化カルシウムCaCl2 (3) ソーダ石灰CaO- NaOH (4) 組成式[実験式] (5) 凝固点降下 (6)分子量
窒素・硫黄・塩素
窒素・硫黄・塩素などの元素が 有機化合物に含まれているかを知りたい場合,以下の ような実験を行うと,その元素の存在が確認できる。
「窒素」
試料と( 1 )を混合して加熱する。試料に窒素が含まれている場合,( 2 )が発生し,濃塩酸と反応して( 3 )が発生する。
「塩素」
黒く焼いた銅線の先に試料をつけてバーナーで加熱する。試料に塩素が含まれている場合,( 4 )ができるため,( 5 )色の炎色反応がおこる。
「硫黄」
ナトリウムの小片を加えて加熱する。試料に硫黄が含まれている場合,( 6 )が生成し,水に溶かして鉛(Ⅱ)イオンを加えると,( 7 )色の硫化鉛(Ⅱ)が沈殿する。
(1) ソーダ石灰 (2) アンモニア NH3 (3) 白煙 (4) 塩化銅(Ⅱ) Cu2O (5) 青緑 (6) 硫化ナトリウムNaS (7) 黒
ベンゼン は分子式では( 1 ),組成式では( 2 )で表される。
(1) C6H6 (2) CH
有機化合物のなかには,同じ分子式でありながら分子の構造が異なる化合物が多数存在する。このような化合物を互いに( 1 )という。
異性体の中で原子や原子団のつながり方が異なる化合物を互いに( 2 )という。
さらに,同じ構造式をもつ化合物の中で,原子や原子団の並び方が空間的に異なる場合があり,このような化合物を互いに( 3 )という。
(1) 異性体 (2) 構造異性体 (3) 立体異性体
異性体のうちで分子の構造式が異なる異性体を構造異性体という。一方,原子のつながり方や,結合の種類は同じであるが立体構造が異なるために生じる異性体を( 1 )異性体という。
(1)異性体には、二重結合に対する置換基の配置の違いに由来する( 2 )異性体や不斉炭素原子の存在による( 3 )異性体などがある。
(1) 立体 (2) 幾何[シス-トランス] (3)光学
原子のつながり方や結合の種類は同じであるが,原子または原子団の配置が立体的に異なるために生じる異性体を( 1 )異性体という。(1)異性体には,( 2 )異性体や( 3 )異性体などがある。(2)異性体の例として,1,2-ジブロモエチレン (BrCH=CHBr)が ある。この例では,炭素-炭素二重結合を軸として2個の臭素原子が同じ側に位置している( 4 )形と, 反対側に位置している( 5 )形が存在する。
(1) 立体 (2) 幾何[シス-トランス] (3) 光学[鏡像] (4) シス (5) トランス
分子式も構造式も同じであるが立体構造が異なる場合,立体異性体という。一般に炭素原子間の二重結合はそれを軸として( 1 )することができないので( 2 )異性体が存在する。分子式 C4H4O4 で表されるジカルボン酸(2価カルボン酸)には化合物( 3 )(トランス型)と、化合物( 4 )(シス型)の2種類の(2)異性体が存在する。
(1) 回転 (2) 幾何[シスートランス] (3) フマル酸 (4) マレイン酸
HOOC-CH=CH-COOH の示性式をもつ不飽和ジカルボン酸には( 1 )(トランス型)と、化合物( 2 )(シス型)の2種類の( 3 )異性体が存 在する。
(1) フマル酸 (2) マレイン酸 (3) 幾何
乳酸には結合する4つの基(原子または原子団)がすべて異なる炭素原子が存在する。このような炭素原子を( 1 )炭素原子といい, 1 個の(1)炭素原子が存在すると2種類の( 2 )異性体が存在する。(2)異性体はほとんどの物理的性質や化学的性質は同じであるが,平面偏光に対する性質や生理的性質 が異なる。
(1) 不斉 (2) 光学
4つの異なる原子または原子団が結合している炭素原子を( 1 )という。1個の(1)をもつ化合物は,平面偏光に対する性質の異なる一対の( 2 )をもつ。
(1) 不斉炭素原子 (2) 光学異性体(鏡像異性体)
1つの炭素原子に異なる4つの官能基または原子が結合した化合物には鏡に対する実像(実体)とその鏡像の関係にある組合せがあり,それらは互いに( 1 )であるという。
(1) 光学異性体
分子式 C3H6O3 で表されるヒドロキシ基をもつ脂肪族カルボン酸には,( 1 )種類の構造異性体が存在するが,不斉炭素原子をもつものは( 2 )である。(2)分子には,重ね合わすことができない実物と鏡像の関係にある立体異性体である( 3 )異性体が存在する。
(1) 2 (2) 乳酸 (3) 光学
アラニンの光学異性体を図で表した。図中の( 1 )~( 3 )に あてはまる原子または原子団を化学式で記せ。
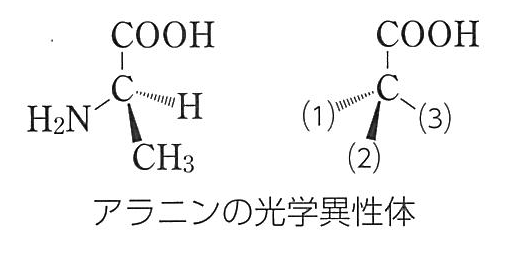
(1) H (2) CH3 (3) NH2
1つの化合物に不斉炭素原子がn個存在する場合,理論的には( 1 )異性体は( 2 )種類存在することになる。
(1) 光学 [鏡像] (2) 2n
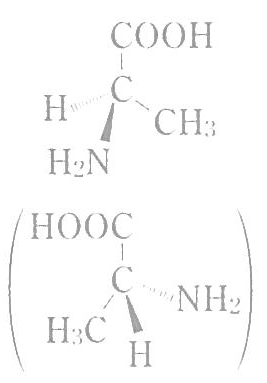
図に示した化合物のもう一方の光学異性体の立体的な構造を,図の例にならって示せ。解答は,3個の炭素原子を紙面上に置いたときの構造で示すこと。
![]()
分子式 C4H10 に考えられる構造異性体は( 1 )個 である。
(1) 2
分子式 C5H12 に考えられる構造異性体は( 1 )個
である。
(1) 3
分子式 C6H4 に考えられる構造異性体は( 1 )個である。
(1) 5
プロパンの水素原子2個をそれぞれ塩素原子で置換した化合物は何種類あるか。ただし,光学異性体を除 く。
4
不斉炭素原子をもつ鎖式飽和炭化水素のうち,最も炭素数の少ないものは炭素数がいくつか。
7
分子式 C4H8Cl2 のジクロロアルカンには構造異性体が何個存在するか。ただし,立体異性体は含めないものとする。
9
分子式 C4H8で示されるアルケンの異性体の数は,立体(幾何)異性体を考慮した場合 ( ) 種である。
4
分子式 C5H10 で表されるアルケンのすべての異性体 は( 1 )個となる。
(1) 6
分子式 C4H10O で表される化合物の中で,金属ナトリウムと反応して水素を発生する化合物には,光学異性体を含めて( 1 )個の異性体が存在する。一方,同 じ分子式で表される化合物Aは, 分子中にメチル基を3個もち,金属ナトリウムと反応しない。
(1) 5
分子式が C5H12O である化合物には,光学異性体を無視すると( 1 )種類の構造異性体が存在する。これらの( 1 )種類の構造異性体について考えてみよう。これらの異性体のうち,( 2 )種類はナトリウ ムと反応して水素を発生するが,他はナトリウムと反応しない。ナトリウムと反応する異性体の中で,不斉炭素原子をもつ化合物は( 3 )種類ある。
(1) 14 (2) 8 (3) 3
分子式 C3H6O2で表されるエステルは( 1 )種類 ある。
(1)2


