一問一答『高校化学/無機/気体の製法』
2020年 月 日 無機1314~1343
(1) 硫化水素H2S (2) 黒 (3) 硫化銅(Ⅱ)CuS
(1) 硫化水素H2S
(1) 腐卵 (2) 硫化水素H2S
(1) 二酸化炭素CO2 (2) 無 (3) 無 (4) 弱酸
(1) 二酸化硫黄SO2
(1) 無 (2) 刺激 (3) 軽 (4) 塩化アンモニウムNH4Cl (5) 水酸化カルシウム (6) 上方
(1) アンモニア (2) 加熱 (3) 塩化水素HCl
(1) 水素H2
(1) 水素H2
(1) 二酸化硫黄SO2 (2) 硫酸銅(Ⅱ)CuSO4 (3) 酸化
(1) 一酸化窒素NO (2) 二酸化窒素NO2 (3) 窒素 (4) 希硝酸HNO3 (5) 濃硝酸HNO3 (6) 赤褐 (7) 四酸化二窒素N2O4 (8) 無
(1) 二酸化硫黄SO2 (2) 酸化 (3) 硫黄S
(1) e 水銀Hg
Fe、Ni、Alは濃硝酸と不動態をつくる。
(1) 塩素Cl2 (2) 塩化水素HCl (3) 塩化水素HCl (4) 水H2 (5) 水蒸気 (6) 濃硫酸H2SO4 (7) 下方
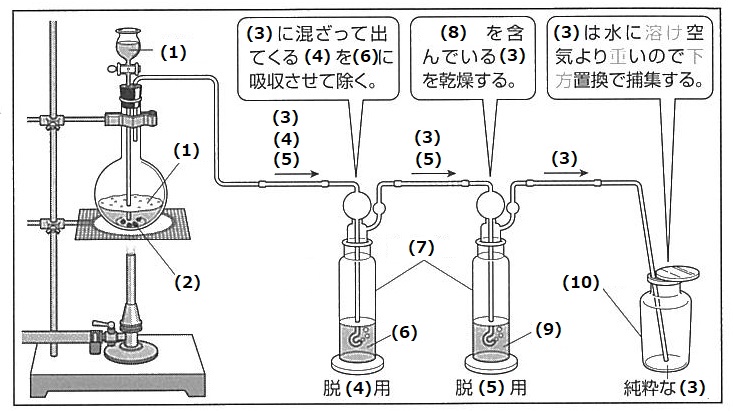
(1) 濃塩酸HCl (2) 酸化マンガン(Ⅳ)MnO2 (3) Cl2 (4) HCl (5) H2O (6) 水 (7) 洗気びん (8) 水蒸気 (9) 濃硫酸 (10) 集気びん
ふたまた試験管と塩酸、( 1 )を使って以下の実験を行った。
実験 A,Bそれぞれに( 2 )と( 3 )を入れた後、(3)をBからAへ移すと、黄緑色の気体( 4 )が発生した。
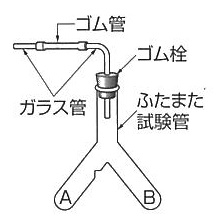
(1) さらし粉CaCl(ClO)・H2O (2) さらし粉CaCl(ClO)・H2O (3) 塩酸HCl (4) 塩素Cl2
さらし粉に塩酸を加えて発生する気体( 1 )は、赤いバラの花を( 2 )させる。(1)は毒性が強いので( 3 )内で( 4 )しながら使う。
(1) 塩素Cl2 (2) 脱色 (3)ドラフト (4) 換気
( 1 )は過酸化水素H2O2の水溶液に、触媒である( 2 )を加えると発生する
(1) 酸素O2 (2) 酸化マンガン(Ⅳ)MnO2
酸素O2は、乾燥空気の体積の約( 1 )%を占める気体である。酸素は、実験室においては( 2 )の水溶液に触媒として( 3 )または( 4 )または( 5 )(順不同)を加える。
(1) 20 (2) 過酸化水素H2O2 (3) 酸化マンガン(Ⅳ)MnO2 (4) 塩化鉄(Ⅲ)FeCl3 (5) カタラーゼ
気体の発生には濃硫酸の( 1 )性や( 2 )作用を利用する場合がある。
(1) 不揮発 (2) 脱水
塩化ナトリウムに濃硫酸を加えて穏やかに加熱し、気体( 1 )を得た。これは濃硫酸の( 2 )が約300℃である( 3 )を利用した反応である。
(1) 塩化水素HCl (2) 沸点 (3) 不揮発性
気体( 1 )は、塩化ナトリウムに濃硫酸を加えて加熱することによって得られる
(1) 塩化水素HCl
気体( 1 )は、ホタル石(化学式( 2 ))に硫酸を作用させるとえられる。
(1) フッ化水素HF (2) CaF2
( 1 )はギ酸に濃硫酸を加えて加熱すると発生する。
(1) 一酸化炭素CO
図の装置で化合物( A )と濃硫酸を加え170℃で加熱することで( 1 )を発生させた。これは濃硫酸の( 2 )作用を利用したものである。
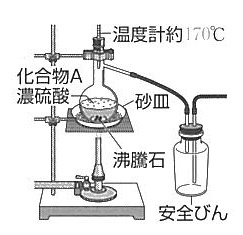
(A) エタノールCH3―CH2―OH (1) エチレン (2)脱水
気体( 1 )は、空気の約20%(体積)を占め、実験室では塩素酸カリウム(化学式( 2 ))と( 3 )の混合物を加熱して発生させる。
(1) 酸素O2 (2) KClO3 (3) 酸化マンガン(Ⅳ)MNO2
窒素は、実験室では亜硝酸アンモニウム(化学式( 1 ))水溶液を加熱して発生させる。この反応の化学反応式は
(1) → ( 2 ) + 2( 3 )
(1) NH4NO2 (2) N2 (3) H2O
図は( 1 )の装置の図である。この装置を用いて硫化鉄(Ⅱ)と希硫酸の反応により( 2 )を発生させた。
はじめに( 3 )の栓をはずし( 4 )の中に硫化鉄(Ⅱ)の小塊を適量入れた。
次に(3)の栓を取り付け、( 5 )および( 6 )(順不同)の栓が閉じていることを確認し、( 7 )に希硫酸を満たした。
( 8 )の栓を開くと、希硫酸は装置内部の空気を押し出しながら( 9 )を満たした後、硫化鉄(Ⅱ)に触れ(2)を発生した。
発生した(2)はGにゴム管で連結したガラス管を通じて捕集した。
Gの活栓を閉じると、(2)の発生はしばらく停止した。
この実験で発生した(2)の密度は空気の密度より( 10 )く、色は( 11 )色で( 12 )のような臭いがある。また、この気体は水に溶解し、わずかに電離して( 13 )性を示す。
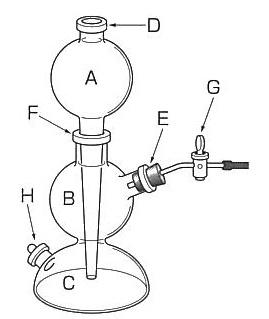
(1) キップ (2) 硫化水素H2S (3) E (4) B (5) G (6) H (7) A (8) G (9) C (10) 大き (11) 無 (12) 腐った卵 (13) 弱酸
次の化合物1molがすべて反応したとき、反応のしくみ、発生する気体と、その物質量を答えなさい。
① 硫化鉄(Ⅱ)FeS1molに希硫酸を加える。
② 塩素酸カリウムKClO31molに触媒である酸化マンガン(Ⅳ)MNO2を加えて加熱する。
③ 過酸化水素H2O21molを含む水溶液を、触媒である酸化マンガン(Ⅳ)MNO2に加える。
④ 炭酸水素ナトリウムNaHCO31molに希塩酸を加える。
⑤ 亜硫酸水素ナトリウムNaHSO31molに希硫酸を加える。
① 弱酸遊離反応 H2S 1mol
② 熱分解反応 O2 1.5mol
③ 酸化還元反応 O2 0.5mol
④ 弱酸遊離反応 CO2 1mol
⑤ 弱酸遊離反応 SO2 1mol
塩酸を加えた時に酸化還元反応によって気体が発生する物質を選びなさい。
① 亜硫酸水素ナトリウム
② さらし粉
③ 炭酸カルシウム
④ 炭酸水素ナトリウム
⑤ 硫化鉄
② ①③④⑤は酸・塩基反応(弱酸遊離反応)

